Entenda o que é calor latente e como utilizamos ele no dia a dia
O estudo do calor latente é fundamental para compreender diversas situações cotidianas, que vão desde a formação de nuvens até o processo de cozimento dos alimentos. Neste artigo, vamos explorar o que é calor latente, como ele opera e quais são suas principais aplicações na prática.
Por – Redação do Física Curiosa
O calor latente é um fenômeno termoquímico que descreve a quantidade de calor envolvida em um processo de mudança de estado físico de uma substância, como a fusão ou a vaporização.
SAIBA+ 10 Experimentos de Física que você pode fazer
Introdução

Estado físico da matéria
Tipos de estado físico
Os estados físicos fundamentais de uma substância podem variar dependendo de como suas partículas estão agregadas, podendo ser sólido, líquido ou gasoso.
Abaixo, é apresentada a representação da água nos seus três estados físicos:

No estado sólido, as partículas de uma substância apresentam pouca mobilidade e se limitam a vibrações em torno de posições definidas. Portanto, os sólidos possuem forma e volume bem definidos.
No estado líquido, as partículas de uma substância possuem maior liberdade de movimento do que no estado sólido, mas ainda apresentam coesão significativa. Isso significa que os líquidos possuem volume definido, mas sua forma pode variar, adaptando-se à forma do recipiente que os contém.
Já no estado gasoso, as partículas de uma substância estão tão afastadas que as forças de coesão entre elas são muito fracas. Isso resulta em um alto grau de liberdade de movimento, fazendo com que as substâncias no estado gasoso (vapores e gases) não possuam forma nem volume definidos.
Quando uma substância recebe ou cede energia térmica, independentemente do estado físico em que se encontra, pode ocorrer uma alteração na forma de agregação de suas partículas, levando-a a passar de um estado para outro. Essa mudança é conhecida como mudança de estado físico.
SAIBA+ Entenda o que é calor Latente e como ele influencia nos materiais.
Mudanças de estado físico
A fusão é o processo de transição da matéria do estado sólido para o líquido, enquanto a solidificação é a transformação inversa, ou seja, a transição da matéria do estado líquido para o sólido.
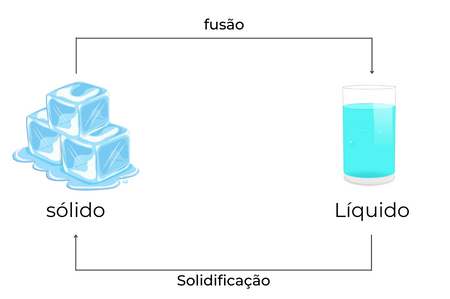
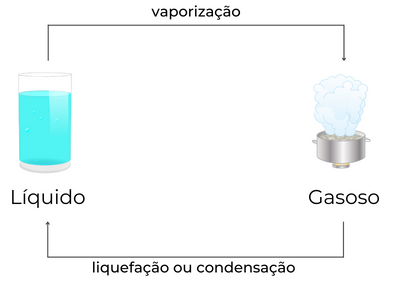
A vaporização é o processo de mudança de estado físico em que uma substância líquida passa para o estado gasoso. O processo inverso é conhecido como liquefação ou condensação, em que uma substância gasosa é transformada em líquido.
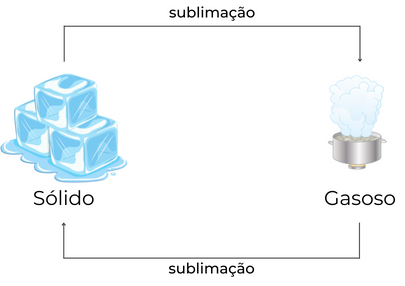
A sublimação é a passagem do estado sólido para o gasoso, sem que determinada substância passe pela fase intermediária, a líquida. A transformação inversa também é denominada sublimação.
SAIBA+ Entenda o que é calor Latente e como ele influencia nos materiais.
Calor Latente, o que é?
Definição
O calor latente é a quantidade de calor necessária para que ocorra uma mudança de estado físico de uma substância, sem que haja variação de temperatura.
Isso significa que, durante esse processo, a energia térmica fornecida não é usada para aumentar ou diminuir a temperatura da substância, mas sim para romper ou formar ligações químicas entre as moléculas que compõem a substância.
Existem três tipos de mudanças de estado físico: fusão, vaporização e solidificação. Na fusão, por exemplo, ocorre a passagem da substância do estado sólido para o líquido, e é necessário fornecer calor para que isso aconteça.
Durante esse processo, a energia térmica fornecida é usada para romper as ligações químicas entre as moléculas do estado sólido e permitir que elas se movimentem livremente no estado líquido.
O calor latente é uma propriedade específica de cada substância e depende do tipo de mudança de estado físico que está ocorrendo. Esse valor é medido em unidades de energia por unidade de massa, como joules por grama (J/g).
O conhecimento sobre o calor latente é importante em diversas áreas, como a climatologia, a engenharia de alimentos e a indústria química.
Exemplos
- Na climatologia: a formação de nuvens ocorre devido ao processo de condensação, que é uma mudança de estado físico em que o vapor de água se transforma em gotículas de água líquida. Durante esse processo, é liberado calor latente, que pode afetar as condições climáticas de uma região.
- Na engenharia de alimentos: o cozimento dos alimentos é um processo que envolve mudanças de estado físico, como a evaporação da água presente nos alimentos. Durante esse processo, é necessário fornecer calor latente para transformar a água em vapor e permitir que o alimento cozinhe.
- Na indústria química: a separação de substâncias em uma mistura pode ser realizada por meio de processos de destilação, que envolvem mudanças de estado físico como a vaporização e a condensação. Durante esses processos, o calor latente é utilizado para separar os componentes da mistura com base em suas propriedades físicas.
Esses são apenas alguns exemplos de como o calor latente é utilizado em diferentes áreas. É importante ressaltar que o conhecimento sobre essa propriedade é fundamental para entender diversos processos físicos e químicos que ocorrem ao nosso redor.
SAIBA+ Entenda o que é calor Latente e como ele influencia nos materiais.
Tipos de Calor Latente
Existem três tipos de calor latente: o calor latente de fusão, o calor latente de vaporização e o calor latente de solidificação.
Calor Latente de fusão
O calor latente de fusão é a quantidade de calor necessária para que ocorra a mudança de estado físico de uma substância do estado sólido para o líquido, sem que haja variação de temperatura. Durante esse processo, a energia térmica fornecida é usada para romper as ligações químicas entre as moléculas do estado sólido e permitir que elas se movimentem livremente no estado líquido.
Calor Latente de vaporização
O calor latente de vaporização é a quantidade de calor necessária para que ocorra a mudança de estado físico de uma substância do estado líquido para o gasoso, sem que haja variação de temperatura. Durante esse processo, a energia térmica fornecida é usada para romper as ligações químicas entre as moléculas do estado líquido e permitir que elas se transformem em vapor.
Calor Latente de solidificação
O calor latente de solidificação é a quantidade de calor liberada quando uma substância passa do estado líquido para o sólido, sem que haja variação de temperatura. Durante esse processo, a energia térmica é liberada à medida que as ligações químicas são formadas entre as moléculas do estado líquido e elas se organizam em um padrão cristalino no estado sólido.
É importante ressaltar que esses valores de calor latente são específicos para cada substância e dependem das condições em que ocorrem as mudanças de estado físico, como a pressão e a temperatura.
SAIBA+ Entenda o que são ondas transversais, longitudinais e mistas
Como calcular o Calor Latente?
Conceitos de fórmulas
A energia térmica é a energia cinética que faz as partículas de um corpo se agitarem, juntamente com a energia potencial de agregação que determina o estado físico do corpo.
Para um estado de agregação específico, há um limite de temperatura para a agitação das partículas do corpo. Esse limite é a temperatura de mudança de estado físico, que depende da substância e da pressão sobre o corpo.
Por exemplo, a água muda de estado físico a 0°C e 100°C sob pressão normal, correspondendo às temperaturas de fusão-sólido e vaporização-liquefação, respectivamente.
Experimentalmente, podemos concluir que a quantidade de calor necessária para provocar uma mudança de estado é diretamente proporcional à massa da porção da substância que sofre a transformação.
Portanto, se a massa do corpo que precisa de uma quantidade Q de calor para sofrer uma mudança de estado total é m, então a expressão correta é:
![]()
A grandeza L é conhecida como calor latente, e sua magnitude é determinada pelo material do qual o corpo é composto, a mudança de estado pela qual o corpo passa e a temperatura na qual essa mudança ocorre.
Por exemplo, para a água, o calor latente de fusão-sólido a 0°C é de cerca de 80 cal/g, enquanto o calor latente de vaporização-liquefação a 100°C é de aproximadamente 540 cal/g.
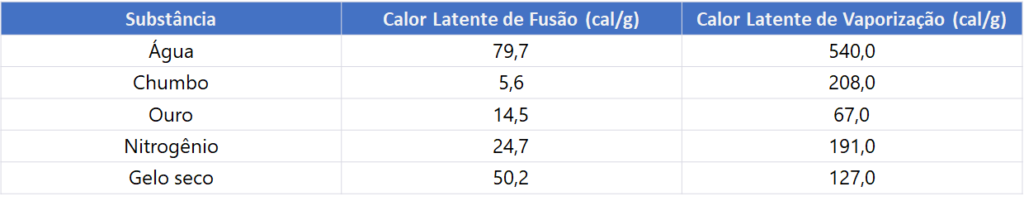
Assim, é possível afirmar que:
O calor latente de fusão (ou solidificação) de uma substância indica a quantidade de calor que cada unidade de massa precisa receber (ou ceder) para que ocorra a mudança de estado físico de sólido para líquido (ou vice-versa).
Por outro lado, o calor latente de vaporização (ou liquefação) de uma substância indica a quantidade de calor que cada unidade de massa precisa receber (ou ceder) para que ocorra a mudança de estado físico de líquido para gasoso (ou vice-versa).
SAIBA+ Conheça as 04 forças da natureza
Calor Latente de fusão (ou solidificação)
Para melhor exemplificar, suponha que um bloco de gelo seja aquecido de -40 °C até 60 °C, vamos analisar por partes esse aquecimento:
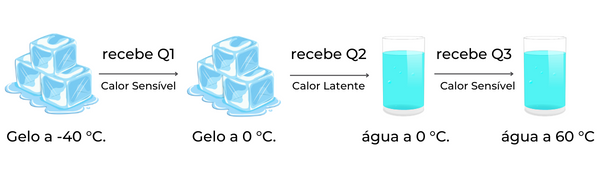
A fim de calcular o total de calor (Q) recebido pelo sistema, utilizamos as fórmulas do calor sensível e do calor latente:
![]()
![]()
Calor Latente de vaporização (ou liquefação)
Para exemplificar esse processo, podemos considerar o aquecimento de um bloco de gelo de massa m, que passa por diferentes fases enquanto é aquecido de -40°C até 120°C em pressão ambiente. Neste contexto, é possível observar como a temperatura afeta a substância em questão e quais são as mudanças que ocorrem em cada uma das etapas desse processo de aquecimento:

O caso em questão é similar ao anterior, podemos utilizar as mesmas equações e seguir a mesma linha de raciocínio:
![]()
![]()
Conclusão
Em conclusão, o calor latente é um conceito fundamental em termodinâmica e tem muitas aplicações práticas em diversas áreas, desde a engenharia até a meteorologia.
Entender o calor latente é crucial para a compreensão de processos como a mudança de fase de uma substância e o armazenamento de energia térmica em sistemas termodinâmicos. Além disso, a capacidade de calcular e medir o calor latente é essencial para a otimização de muitos processos industriais, como a fusão de metais e a produção de alimentos congelados.
Portanto, a compreensão e o uso adequado do calor latente são fundamentais para o desenvolvimento de tecnologias mais eficientes e sustentáveis e para o avanço da ciência em geral.
Para estudos e referências:
Livro de Termodinâmica Capa comum – por Yunus A. Çengel e Michael A. Boles